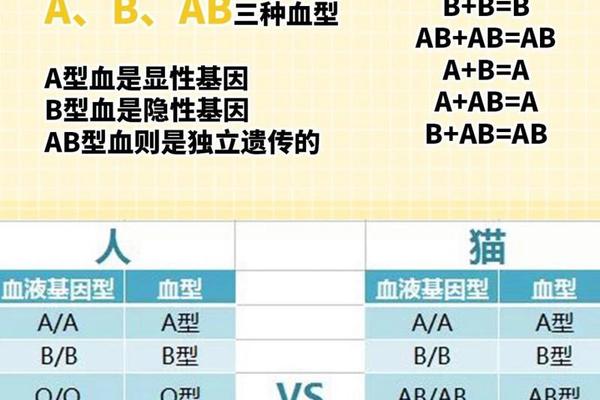
在自然界中,A型血并非人类独有。灵长类动物中,黑猩猩和大猩猩的血液系统均存在与人类ABO血型相似的分型机制。例如,黑猩猩群体中约30%的个体表现为A型血,其红细胞表面携带的A抗原与人类A型血的抗原结构具有同源性。猫科动物的血型系统则更为特殊,93%的家猫属于A型血,而纯种猫(如波斯猫、暹罗猫)中B型血比例显著升高,AB型极为罕见。这种分布特征表明,A型血在动物界的普遍性与物种进化过程中环境适应性存在关联。
反刍动物的血型系统则呈现更高复杂性。牛的血液中已发现超过40种抗原组合,其中B型血占比最高,而A型仅存在于部分品种。马的血型系统中虽存在类似A抗原的结构,但其免疫反应机制与人类存在本质差异——马的血清不会自然产生针对外来抗原的抗体,仅在输血或感染后可能触发免疫应答。这种生物学特性为跨物种输血研究提供了独特视角。
A型血的遗传机制解析
人类A型血的遗传遵循孟德尔定律,由位于9号染色体上的ABO基因调控。当个体携带至少一个A等位基因(AA或AO型)时,红细胞表面会表达A抗原。父母血型组合中,若一方为AA型,另一方为任意血型,子代必定携带A型基因;若父母均为AO型,则有25%概率生育O型血后代。这种显性遗传特征使得A型血在全球人口中占比达28%-40%,成为仅次于O型的第二大血型。
特殊情况下,孟买血型(hh型)会干扰常规遗传规律。这类个体虽携带A基因,但因缺乏H抗原前体物质,红细胞无法正常表达A抗原,在常规检测中呈现伪O型特征。2021年国内报道的案例显示,B型血与伪O型血(实际为孟买型携带A基因)结合可能生育出A型血后代,这种遗传异常概率仅约十万分之一。这提示临床输血前必须进行精准血型鉴定,避免误判风险。
跨物种输血的可能性探索
历史上最早的异种输血实践可追溯至1667年,法国医生让-巴蒂斯特·德尼将羊血输入人体,虽取得短期疗效但最终导致受体死亡。现代研究发现,猪的红细胞与人类存在形态学相似性——直径7-8μm,寿命约120天,且通过基因编辑可消除α-半乳糖抗原,使异种输血排斥反应降低70%。这种技术突破为缓解血库短缺提供了新思路,但跨物种病原体传播风险仍需长期监测。
灵长类动物的输血研究揭示更深层的进化密码。恒河猴的Rh抗原与人类完全同源,这种蛋白质的同源性支持了达尔文共同祖先理论。对黑猩猩血型的大规模测序显示,其A型抗原的编码基因与人类差异仅3个碱基对,这种高度保守性暗示A型血可能在500万年前的人猿分化时期就已存在。这些发现为研究血型系统的物种演化提供了分子生物学证据。
从灵长类到家养宠物,A型血在动物界的广泛存在揭示了生命进化中的保守选择机制。其遗传规律虽遵循经典模型,但孟买血型等特殊案例警示我们需用动态视角理解血型系统。异种输血研究取得的突破性进展,尤其是猪红细胞改造技术的成熟,为未来血液替代品开发指明方向。

建议未来研究可从三方面深入:第一,建立跨物种血型数据库,系统分析抗原结构差异;第二,开发新型基因编辑工具,精准调控异种红细胞抗原表达;第三,加强血型与疾病易感性关联研究,特别是动物模型中A型血与传染病的相互作用机制。这些探索不仅将深化对生命本质的理解,更可能为临床医学带来革命性突破。


