人类对血型与寿命关系的探索,始终交织着科学理性与民间想象的张力。近年来,某些研究指出B型血人群可能存在更高的疾病风险,甚至与寿命缩短存在关联,而血型亚型的发现更让这一命题复杂化。例如,B(A)亚型等罕见血型因抗原表达的异常,可能通过凝血机制、炎症反应等途径间接影响健康。这一现象背后,既有基因遗传的生物学基础,也涉及环境与生活方式的交互作用。现有研究结论的碎片化与矛盾性,使得这一话题仍处于争议的漩涡之中。
血型遗传与亚型机制
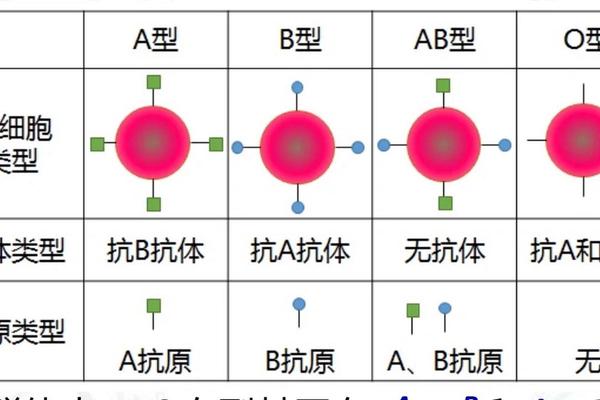
ABO血型系统的遗传由9号染色体上的基因决定,其中A和B为显性基因,O为隐性基因。B亚型(如B(A)亚型)的产生源于基因突变导致的糖基转移酶活性异常,例如B(A)04等位基因会在红细胞表面同时表达弱化的A抗原和正常B抗原。这种分子层面的变异不仅影响输血相容性,更可能改变血液黏稠度、炎症因子水平等生理指标。例如,B(A)亚型个体的红细胞膜抗原结构异常,可能干扰血小板与血管内皮的相互作用,从而增加微循环障碍风险。
从进化角度看,B型血的出现晚于A型血,其消化系统对动物蛋白的适应能力更强,但这也意味着在饮食结构剧变的现代社会,B型血人群更易因高脂饮食引发代谢紊乱。日本学者古川竹二曾提出B型血人群外向敏感的性格特征,但后续研究显示,这种关联缺乏遗传学证据支撑,更多是统计学上的巧合。值得注意的是,亚型血人群的基因多态性可能进一步放大此类风险,例如B(A)亚型携带者的凝血因子Ⅷ水平异常,已被证实与血栓性疾病存在关联。
疾病易感性的双重路径
多项流行病学研究揭示了B型血与特定疾病的关联。2019年《糖尿病学》杂志的一项8万人队列研究表明,B型血人群患2型糖尿病的风险比其他血型高21%,其机制可能与胰岛素受体信号通路的基因调控相关。B型抗原与幽门螺杆菌的结合能力较弱,导致此类人群消化道溃疡发病率较低,却可能因此忽视早期感染症状,反而增加胃癌风险。
在心血管领域,矛盾结论尤为突出。中国2014年对心血管疾病患者的血型分析发现,B型血男性冠心病发病率达10.7%,且随年龄增长该比例显著下降,提示B型血可能加速动脉粥样硬化进程。但美国学者对60万人的研究却显示,B型血与早发性中风无显著关联,反而是A型血人群风险更高。这种差异可能源于人群遗传背景的异质性,例如东亚人群的FUT2基因多态性可能放大B型血的代谢缺陷。
统计学数据的矛盾性
长寿人群的血型分布研究呈现显著地域差异。1981年长春地区调查显示,90岁以上老人中A型血占比最高,O型血反而较少;而2001年新疆和田地区的维吾尔族长者中,B型血比例高达42%,远超其他血型。这种矛盾暗示血型与寿命的关联可能被环境因素掩盖。例如,传统农耕社会的B型血人群因体力劳动强度高、饮食结构单一,其代谢优势反而转化为健康负担。
跨国研究的对比更具启示性。英国大学对189名痴呆患者的分析发现,O型血人群的认知衰退风险最低,而B型血人群的神经退行性疾病发生率并无特异性。美国数学家魏斯贝格对5000人的问卷调查虽得出B型血平均寿命77岁的结论,但其样本选择偏倚(如未区分亚型)遭到学界质疑。这些矛盾提示,单纯依靠统计学相关性难以构建因果链条,必须结合分子机制研究。
超越血型的健康密码

基因与环境交互作用的研究为破解血型谜题提供新思路。端粒长度作为衰老的生物标志物,在B型血人群中呈现更快的缩短速率,这可能与慢性炎症状态加速细胞分裂有关。B型血个体的肠道菌群组成差异(如拟杆菌门丰度较高)可能通过肠脑轴影响免疫调节功能。这些发现表明,血型对寿命的影响需通过多组学整合分析才能准确评估。
健康管理策略需因“型”制宜。针对B型血人群,建议加强血糖监测与心血管筛查,尤其对于B亚型携带者,定期检测凝血功能至关重要。饮食方面,减少红肉摄入、增加膳食纤维可缓解代谢负荷。值得关注的是,某些传统文化中的养生实践(如地中海饮食)与血型适应性高度契合,这为个性化预防医学提供启示。
现有证据表明,B型血及亚型人群的寿命特征受多因素调控:基因突变导致的抗原异常可能增加特定疾病风险,但环境适应性与行为选择才是决定健康结局的关键。未来研究需聚焦三方面:一是建立大样本亚型血人群队列,解析罕见血型的分子病理机制;二是开发血型特异性生物标志物,实现疾病早期预警;三是构建基因-环境交互作用模型,为精准预防提供依据。正如诺贝尔奖得主彼得·梅达沃所言:“寿命是基因交给环境的抵押品。”唯有打破生物学决定论桎梏,才能揭开人类长寿的真正密码。


