在人类复杂的生命系统中,血型不仅是遗传密码的独特表达,更是临床医学中维系生命的重要纽带。当我们在体检报告上看到"A型RH+"的标注,这串字符背后蕴含着红细胞表面抗原的精密编码体系——既包含ABO血型系统中的A抗原特征,又携带Rh血型系统中的D抗原标记。这种双重血型分类标准的确立,源自二十世纪医学家对输血反应机制的突破性发现,如今已成为现代医疗体系中不可或缺的临床指导依据。
一、血型系统的双重密码
ABO血型系统与Rh血型系统构成了人类血液分类的两大基石。前者根据红细胞表面A、B抗原的有无将人群划分为A型、B型、AB型和O型四大类,后者则依据D抗原的存在与否分为Rh阳性(RH+)和Rh阴性(RH-)。A型RH+即表示个体在ABO系统中表现为A型血,同时在Rh系统中携带D抗原。
这种双重分类体系的临床意义远超普通认知。统计数据显示,我国汉族人群中Rh阳性占比高达99.7%,而Rh阴性血型因稀缺性被称为"熊猫血",其分布存在显著地域差异——新疆少数民族中Rh阴性比例可达5%,这提示血型分布与族群迁徙、地域隔离存在密切关联。值得注意的是,除ABO和Rh系统外,目前已发现35种人类血型系统,如Kell、Duffy等系统,但这些系统的临床重要性相对较低。
二、输血医学的生命法则
在临床输血实践中,A型RH+血型遵循严格的相容性原则。该血型个体可接受A型或O型的Rh阳性血液,其红细胞可输给A型及AB型的Rh阳性受血者。这种限制源于抗原-抗体反应的生物学机制:当Rh阴性个体首次接触Rh阳性血液时,虽不会立即产生溶血反应,但会产生免疫记忆,二次输入时将引发致命性的溶血反应。
特殊情况下,医学允许突破常规输血原则。对于Rh阴性危急患者,在无法获得同型血液时,可一次性输注Rh阳性血液挽救生命。这种决策背后是风险效益的精准权衡——约70-85%的Rh阴性个体输入阳性血液后不会产生抗D抗体,但需承担30%左右的致敏风险。近年研究揭示,抗D抗体的产生概率与输入红细胞数量正相关,这为临床制定最小有效输血量提供了理论依据。
三、遗传编码的世代传递
Rh血型的遗传遵循孟德尔隐性遗传规律。当父母双方均携带Rh阴性基因时,子女必然表现为Rh阴性;若父母中一方为Rh阳性,则子女可能继承显性阳性基因。基因测序技术证实,RhD基因位于1号染色体短臂,其缺失或突变是导致Rh阴性的分子基础。值得关注的是,约0.2%-1%的Rh阳性人群存在D抗原变异体,这类"弱D型"个体的临床处理仍存在争议。
血型抗原的表达具有发育时序特征。胚胎期Rh抗原的表达早于ABO抗原,这解释了为何Rh血型不合的母婴溶血可发生在首次妊娠,而ABO系统溶血多发生于再次妊娠。分子生物学研究显示,Rh抗原不仅是简单的表面标记,还参与维持红细胞膜稳定性,这为Rh阴性个体红细胞寿命较短的现象提供了科学解释。
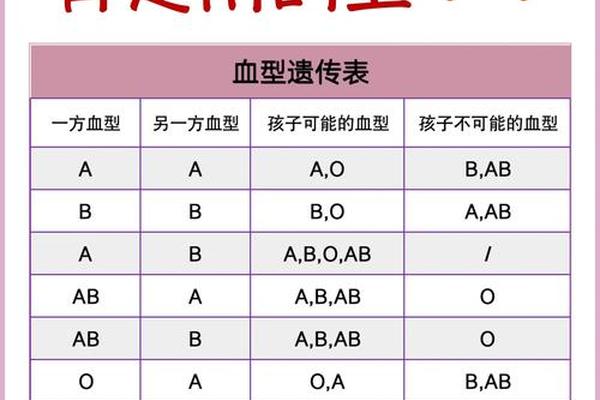
四、疾病易感性的血型图谱
流行病学研究揭示了血型与疾病易感性的微妙关联。A型血人群的胃癌发病率较其他血型高20%,这可能与A抗原促进幽门螺杆菌定植相关。在心血管疾病领域,非O型血的静脉血栓风险较O型血增加1.8倍,这种差异源自ABO抗原对凝血因子Ⅷ的稳定作用。
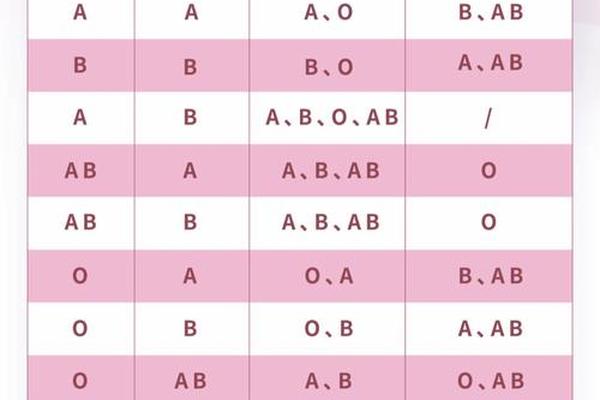
妊娠医学领域的研究更为引人注目。Rh阴性孕妇孕育Rh阳性胎儿时,胎母输血综合征发生率达13%,其中0.8%会导致严重的新生儿溶血病。预防性抗D免疫球蛋白的应用使这类并发症发生率降低至0.1%,但基因检测发现,约5%的Rh阴性孕妇存在抗D抗体天然缺失,这为个体化预防提供了新思路。
从输血安全到疾病预防,从遗传咨询到精准医疗,A型RH+血型的研究持续推动着医学进步。未来研究可深入探索血型抗原的免疫调节功能,开发基于血型特征的个性化治疗方案。在基因编辑技术突飞猛进的今天,科学家正尝试通过CRISPR技术修饰造血干细胞的血型抗原,这或许将彻底改写输血医学的现有格局。对血型系统的深入理解,不仅关乎个体健康,更是人类探索生命奥秘的重要窗口。


