血液的抗原与抗体匹配是输血安全的核心问题,而ABO血型系统作为人类最早发现且最重要的血型分类标准,其复杂的抗原-抗体反应机制直接影响临床医学实践。在ABO系统中,A型个体的红细胞表面携带A抗原,血清中天然存在抗B抗体;而AB型个体的红细胞同时表达A和B抗原,血清中理论上不含抗A或抗B抗体。亚型的存在、抗体效价差异以及检测方法的局限性,使得实际临床中需对血清抗体特性进行更深入的探讨。
ABO血型系统的抗原与抗体基础
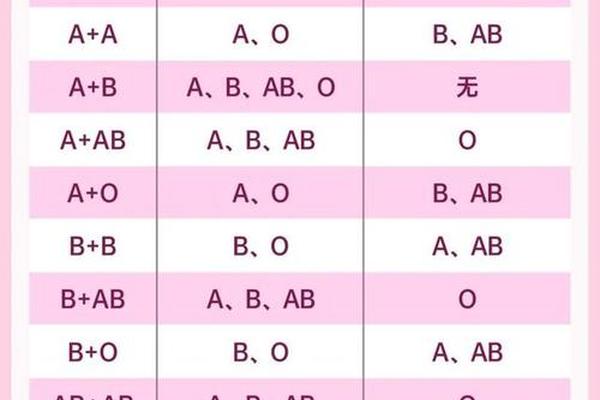
ABO血型系统由红细胞膜上的A、B抗原决定,其抗原合成基于前体物质H抗原。A型个体的A抗原由A基因编码的α-1,3-N-乙酰半乳糖胺转移酶催化形成,而B抗原则由B基因编码的α-1,3-D-半乳糖转移酶催化。血清中的抗体则呈现互补特性:A型血清含抗B抗体,B型含抗A抗体,O型含抗A和抗B抗体,而AB型血清理论上不含有这两种抗体。这种抗原-抗体的对应关系源于免疫系统对非自身抗原的识别,例如A型个体在接触B抗原后,体内会自然产生抗B抗体。
值得注意的是,ABO抗体的性质存在类型差异。抗A和抗B抗体主要为IgM型,分子量较大,无法通过胎盘,因此在新生儿溶血病中作用有限。某些情况下可能产生IgG型抗体,这类抗体可穿过胎盘引发胎儿溶血风险。研究显示,IgG抗体的检测对实验方法敏感度要求更高,例如LISS-凝胶卡法比传统凝聚胺法更易检出低浓度抗体。
A型血清抗体的特性与亚型影响
A型血清中的抗B抗体具有强效价特征,在标准血型鉴定中表现为与B型红细胞的显著凝集反应。A型本身存在超过20种亚型,其中A1和A2亚型占比超过99%。A1型红细胞同时表达A和A1抗原,而A2型仅含A抗原,且抗原密度仅为A1型的20%-25%。这种差异导致A2型血清中可能含有抗A1抗体,约1%-2%的A2个体和22%-26%的A2B个体血清中可检测到此类抗体。
临床输血中,A亚型的抗原强度差异可能引发误判。例如,A2或A2B型红细胞因抗原性弱,使用标准抗A试剂检测时可能被误判为O型或B型。此类误判若未被交叉配血试验发现,输入O型受血者体内可能引发溶血反应。国际输血协会建议对A型供血者进行亚型筛查,尤其是多次输血或存在输血反应史的患者。
AB型血清的抗体特殊性及临床争议
AB型个体因红细胞同时表达A和B抗原,血清中通常不含抗A和抗B抗体,这一特性使其曾被称为“万能受血者”。近年研究揭示了AB型血清抗体的复杂性。AB型中存在A1B和A2B亚型差异,A2B型红细胞抗原数量显著低于A1B型,其血清中可能含有抗A1抗体。约0.1%的AB型个体会产生不规则抗体,如抗H抗体(孟买型)或抗Lewis抗体,这些抗体可能引发交叉配血不相容。
一项针对87例输血患者的抗体筛查发现,使用高灵敏度检测方法时,10例AB型患者血清中检出低效价抗A或抗B抗体,提示常规检测可能存在漏检风险。这颠覆了传统认知,表明AB型血清的“无抗体”特性并非绝对。AB型个体接受大量异型输血时,供血者血清中的抗体可能超过受血者血浆的稀释能力,导致迟发性溶血反应。
交叉配血技术的临床决策价值
交叉配血试验是规避输血风险的最后防线,包含主侧(供血者红细胞+受血者血清)和次侧(受血者红细胞+供血者血清)检测。对A型受血者而言,主侧试验需确保供血者红细胞不被自身抗B抗体凝集;而AB型受血者虽然次侧试验允许供血者血清含抗A/B抗体,但需控制输血速度和总量。现代输血医学强调,即使ABO同型输血也必须完成交叉配血,因为亚型差异、抗体变异等因素可能导致理论预测与实际结果不符。
技术进步提升了抗体检测的精确性。比较四种常用方法发现:LISS-凝胶卡法对IgG抗体的检出灵敏度比传统试管法高8倍,特别适用于检测AB型血清中的微量抗体。分子生物学技术可通过分析ABO基因序列(如第6、7外显子突变)预判亚型风险,这对A2B等特殊血型的输血安全具有重要意义。
研究局限与未来方向
当前研究仍存在若干盲区。A亚型的地理分布差异尚未完全明确,中国汉族人群中A2型占比不足1%,但某些民族可达5%,这提示需建立区域性血型数据库。AB型血清中微量抗体的临床意义尚未量化,需要大规模队列研究确定安全输血阈值。基因编辑技术的发展为人工修饰红细胞抗原提供了可能,例如通过CRISPR敲除ABO基因表达,或将成为解决稀有血型输血难题的新方向。
A型与AB型血清的抗体特性既遵循ABO系统的基本规律,又因亚型多样性、检测方法差异等因素呈现复杂表现。临床实践中需摒弃“绝对无抗体”的简单认知,通过高灵敏度检测技术和个体化配血方案保障输血安全。未来研究应聚焦于抗体动态监测技术的开发、人群特异性血型数据库的建立以及基因修饰血源的制备,从而推动输血医学向精准化方向发展。