A型血是ABO血型系统中最为复杂的类型之一,其核心特征在于红细胞表面存在A抗原,而血浆中含有抗B抗体。这种抗原-抗体的双重特性源于基因编码的糖基转移酶作用。A抗原的形成依赖于H抗原的转化,由A等位基因编码的α-1,3-N-乙酰氨基半乳糖转移酶催化完成,将N-乙酰半乳糖胺连接到H抗原的糖链末端。而抗B抗体的产生则与免疫系统的天然防御机制相关,当个体缺乏B抗原时,免疫系统会将其识别为“异物”,从而产生对应的凝集素。
从分子结构来看,A抗原与B抗原的差异仅在于末端糖基的不同。这种微小的化学结构差异却决定了免疫反应的专一性:抗B抗体能够精准识别并攻击携带B抗原的红细胞,导致溶血反应。研究还发现,A型抗原不仅存在于红细胞表面,还广泛分布于上皮细胞、血管内皮细胞及体液中,这使得A型血在器官移植和疾病易感性研究中具有特殊意义。
亚型分类的复杂性与临床意义
A型血并非单一类型,其内部存在超过20种亚型,其中A1和A2亚型占99%以上。A1亚型的红细胞同时携带A和A1抗原,而A2亚型仅表达A抗原,这种差异导致两者在血清学反应中表现不同。例如,A2型个体的血清中可能含有抗A1抗体,当输入A1型血液时可能引发凝集反应。更值得注意的是,A2型红细胞的抗原数量仅为A1型的1/4-1/3,这使得常规血型检测可能将A2型误判为O型,导致输血事故。
弱亚型如A3、Ax等则更具挑战性。以Ax型为例,其红细胞只能被O型血清中的抗-AB抗体微弱凝集,常规检测极易误判为O型。这类亚型的发现揭示了ABO系统的高度复杂性:2016年日本学者通过基因测序发现,某些罕见亚型的形成与糖基转移酶基因的移码突变直接相关。临床统计显示,我国汉族人群中A2亚型占比不足1%,但在输血医学中仍需建立多重检测体系以避免误诊。

健康风险的关联性研究进展
流行病学研究揭示了A型血与特定疾病的显著相关性。哈佛大学公共卫生学院对8.95万名成年人20年的追踪发现,A型血人群患心脏病的风险较O型血高5%,这可能与A型血中低密度脂蛋白胆固醇水平较高有关。在癌症领域,A型血人群的胃癌发病率较其他血型高20%,研究推测这与幽门螺杆菌感染后的免疫应答异常相关——A抗原与细菌脂多糖的分子模拟可能导致慢性炎症。
认知功能研究则呈现矛盾结论。谢菲尔德大学的MRI扫描显示,A型血人群海马区灰质体积较O型血减少12%,理论上可能增加阿尔茨海默病风险。但日本2023年的队列研究却未发现血型与认知衰退的显著关联,提示环境因素可能在疾病发生中起调节作用。这种矛盾性凸显了血型研究需要结合表观遗传学等多维度分析。
输血医学中的特殊考量
在输血实践中,A型血的特殊性要求严格的操作规范。虽然理论上A型受血者可接受A型或O型血液,但O型血浆中的抗A抗体可能引发急性溶血反应。研究显示,当输入O型全血超过1000ml时,受血者血浆中的抗A效价可能升至1:64,导致血红蛋白尿。对于亚型输血更需要谨慎:A2B型血液若误输给A1B型患者,可能因抗A1抗体引发迟发性溶血反应。
新兴技术正在改变输血安全格局。2024年英国学者发现的MAL血型系统,揭示了AnWj抗原缺失可能导致的严重输血反应。该研究通过全外显子测序技术,建立了A型血亚型的快速基因分型方案,使亚型误判率从0.3%降至0.01%。这提示未来血型检测需要整合蛋白组学与基因组学数据,建立多维鉴定体系。
遗传规律与社会认知的演进
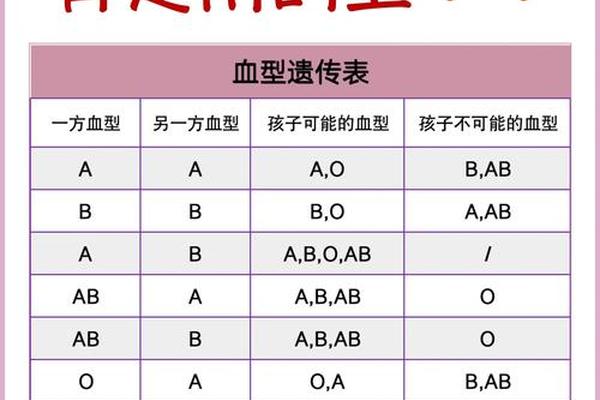
A型血的遗传遵循显性遗传规律,但存在特殊变异现象。当父母基因型为AO与BO时,子代出现AB型的概率达25%,这与传统的显隐性模型相悖,实际由顺式AB基因导致。此类发现不断修正着公众认知:2025年我国血库数据显示,因基因重组产生的罕见A亚型占比已从0.001%上升至0.005%,反映出检测技术的进步。
社会对血型的认知仍存在误区。调查显示,38%的公众误认为O型是“万能供血者”,而忽视其血浆中的抗A/B抗体风险。科普工作需要强调:现代输血医学已淘汰异型输血常规操作,即便是紧急情况,也必须进行抗体效价检测和血液成分分离。
A型血的生物学特性既是生命进化的精妙设计,也是医学研究的复杂课题。从分子层面的糖基转移酶作用,到临床输血的亚型甄别,再到疾病风险的关联机制,A型血研究始终推动着精准医学的发展。当前研究仍需突破三大方向:建立覆盖所有已知亚型的快速检测技术、阐明血型抗原在肿瘤免疫中的调控机制、开发基于血型特征的个性化健康管理方案。正如2024年《新英格兰医学杂志》社论所述:“对ABO系统的深入探索,将为实现真正的个体化医疗提供关键拼图。”未来,随着单细胞测序技术的普及,我们有望解码A型血抗原表达的时空差异性,为疾病预防和诊疗开辟新路径。


