在医学和生物学领域,血型系统的研究始终是理解人类免疫反应和遗传规律的重要基石。当提及“AB血型血清中AB都不凝集”的现象时,其核心指向的是ABO血型系统中的AB型血。这类血型不仅因其独特的抗原-抗体分布模式成为输血医学的关键研究对象,更因其在免疫兼容性上的特殊性引发了广泛关注。本文将深入探讨AB型血的血清学特征、分子机制及其临床应用价值,并揭示其背后的科学逻辑。
一、AB型血的血清学特性
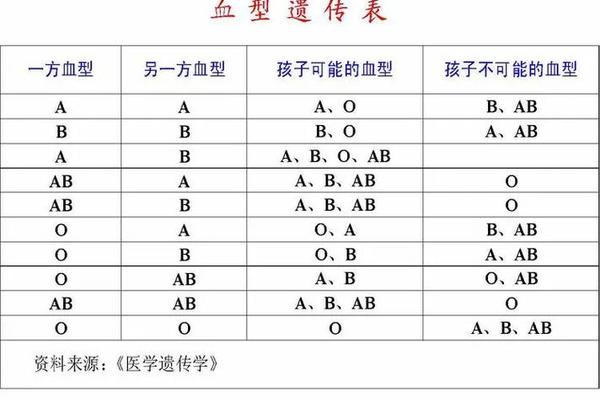
AB型血在ABO血型系统中的独特地位源于其抗原与抗体的特殊组合。根据标准血清学检测,AB型个体的红细胞表面同时存在A和B两种抗原,而血清中既不含有抗A抗体,也不含有抗B抗体。这种“双抗原-无抗体”的特征使得AB型血清在与A型、B型或AB型红细胞混合时均不会发生凝集反应,形成所谓的“AB都不凝集”现象。
从免疫学角度分析,抗体的缺失源于AB型个体在发育过程中免疫系统对自身抗原的耐受性。由于红细胞已携带A和B抗原,免疫系统不会产生针对这些抗原的抗体,从而避免了自体免疫攻击。这种机制在临床交叉配血试验中尤为重要,例如当AB型受血者接受其他血型供血时,其血清不会破坏供血者的红细胞。
二、AB型血的分子遗传学基础
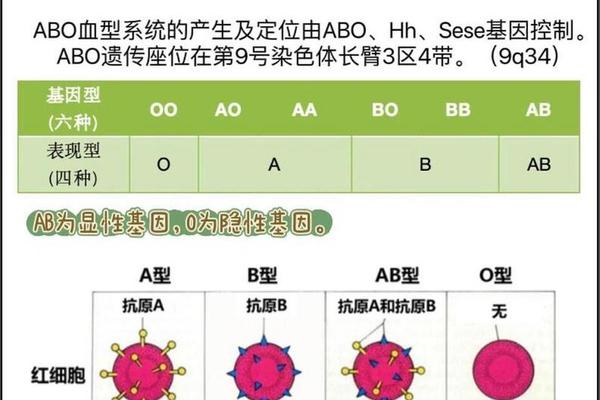
AB型血的抗原表达由9号染色体上的ABO基因调控。该基因的三个主要等位基因(IA、IB和i)通过编码不同的糖基转移酶决定抗原类型。AB型个体通常携带IA和IB两个显性等位基因,其红细胞表面的H抗原被分别转化为A抗原和B抗原。
分子结构研究表明,A抗原的末端糖基为N-乙酰半乳糖胺,B抗原则为半乳糖,而O型血因i基因的无活性仅保留H抗原。这种糖链结构的差异通过抗原-抗体特异性识别机制,直接影响血清学反应的结果。例如,在血型鉴定实验中,AB型红细胞会与抗A和抗B标准血清均发生凝集,而其自身血清不会凝集任何标准红细胞。
三、临床输血中的特殊地位与风险
传统观点将AB型血称为“万能受血者”,因其理论上可接受所有ABO血型的红细胞。现代输血医学强调这一概念的局限性:AB型个体虽无抗A/B抗体,但供血者血清中的抗体仍可能引发溶血反应。例如,当输入大量O型血时,供血者血清中的抗A和抗B抗体会攻击受血者的AB型红细胞。
实际临床操作中,AB型血的输血策略需综合考虑血浆相容性。在紧急情况下,AB型血浆可作为“万能血浆”输注给其他血型患者,因其不含抗A/B抗体。但这种操作需严格控制输注量,并通过交叉配血试验验证兼容性。统计数据显示,AB型患者接受异型输血后发生迟发性溶血反应的概率约为0.03%,提示临床仍需优先选择同型输血。
四、特殊情境下的血清学变异
部分病理或遗传因素可能导致AB型血清学特征的改变。例如,白血病患者可能因造血干细胞异常出现抗原表达减弱,导致血型鉴定结果偏差。罕见的孟买血型(hh表型)个体虽基因型为AB,但因缺乏H抗原前体,红细胞无法合成A/B抗原,血清中反而会出现抗H抗体。
在新生儿溶血病中,AB型母亲若携带免疫性抗A/B抗体(通常因既往异型输血或妊娠引发),可能通过胎盘攻击胎儿红细胞。这类案例的血清学检测需结合抗体效价测定和分子分型技术,以制定精准干预方案。研究显示,AB型孕妇发生新生儿溶血病的概率低于O型孕妇,但一旦发生往往病情更为复杂。
五、未来研究方向与技术革新
随着基因编辑技术的发展,人工调控ABO抗原表达已成为可能。2023年日本学者通过CRISPR技术成功将A型红细胞转化为O型,这一突破为通用血型制品的开发提供了新思路。质谱流式细胞术等新型检测手段能够实现红细胞抗原的定量分析,有助于提高AB型亚类(如A1B与A2B)的鉴别精度。
在临床实践层面,建立基于人群血型数据库的智能输血系统将成为趋势。通过整合ABO血型、不规则抗体筛查和患者免疫史数据,该系统可动态优化血源分配策略,降低AB型患者的输血风险。针对稀有血型群体的冷冻血库网络建设,也将提升特殊医疗情境下的血液保障能力。
AB型血的“AB都不凝集”特性既是免疫耐受的典范,也蕴含着复杂的临床挑战。从分子机制到输血实践,这一血型的独特性质持续推动着血液医学的进步。未来研究需进一步探索ABO抗原的免疫调节机制,开发更安全的异型输血方案,最终实现精准化、个性化的血液治疗目标。


