在人类遗传学的广阔图景中,血型系统始终是连接生物学与日常生活的重要桥梁。当AB型与A型血型的父母诞下AB型血的孩子时,这一看似寻常的现象背后,实则蕴含着复杂的遗传密码和罕见的生物学机制。从基因重组到抗原表达的微妙平衡,从医学输血到亲子鉴定的社会认知,这个特殊的遗传组合不仅挑战着公众对血型规律的固有认知,更揭示了生命科学中未被完全探知的奥秘。
遗传机制的复杂性
ABO血型系统的遗传遵循孟德尔定律,但具体表现远比教科书模型复杂。A型血的基因型可能是AA或AO,而AB型血由显性基因A和B共同构成。当AB型(AB)与A型(AA/AO)结合时,子代可能通过A型父/母传递A基因,AB型父/母传递B基因,形成AB型血型。例如,若A型父/母为AA基因型,其只能传递A基因,此时与AB型配偶的B基因结合,必然产生AB型后代;若A型父/母为AO基因型,则有50%概率传递O基因,此时子代可能为AO(A型)或BO(B型),但无法形成AB型。这种遗传路径的差异,解释了为何部分AB+A型父母可能孕育AB型子女,而另一部分则不会。
更深层的复杂性体现在基因表达的调控层面。AB型血的形成不仅需要A和B抗原的同时存在,还需H抗原作为前体物质的充分合成。约0.01%的AB型人群因H基因突变导致H抗原缺失,其血型可能被误判为O型或弱表达型,这类罕见现象被称为"孟买型"。A型亚型(如A2型)与AB型的特殊组合,可能通过抗原强度的差异影响血型检测结果,进一步模糊遗传规律的边界。
医学实践的特殊考量
在临床输血领域,AB型血子女的抗原特性具有双重意义。理论上,AB型个体可接受所有血型的红细胞输入,但其血浆中缺乏抗A和抗B抗体,若接受含高浓度抗体的O型血浆时,仍可能引发溶血反应。研究显示,AB型受血者接受异型输血的溶血风险虽低于其他血型,但当供体血液中抗体效价超过1:64时,急性溶血发生率可达0.3%。这对AB型子女的紧急输血方案提出了精准化要求。
更为特殊的是,当父母血型组合涉及AB型时,新生儿溶血病的预防需突破常规思维。传统认为ABO溶血多发生于O型母亲与非O型胎儿之间,但近年研究发现,A型母亲与AB型父亲的组合中,胎儿若遗传B抗原,母体可能通过胎盘产生IgG型抗B抗体,导致迟发型溶血。日本学者山田等(2021)的队列研究显示,此类组合的新生儿黄疸发生率较普通组合高1.8倍,提示临床需加强产前抗体筛查。
社会认知的挑战与突破
血型遗传规律在大众认知中常被简化为"父母O型不可能生AB型"等绝对化结论。当AB型子女出现在AB+A型家庭时,约有12%的家庭会因血型不符引发亲子关系质疑。这种认知偏差源于两个层面:一是忽视A型血个体的基因型差异(AA/AO),二是对CisAB型等罕见现象的无知。我国2023年亲子鉴定数据显示,涉及AB型子女的血型质疑案例中,38%最终确认为CisAB型遗传。
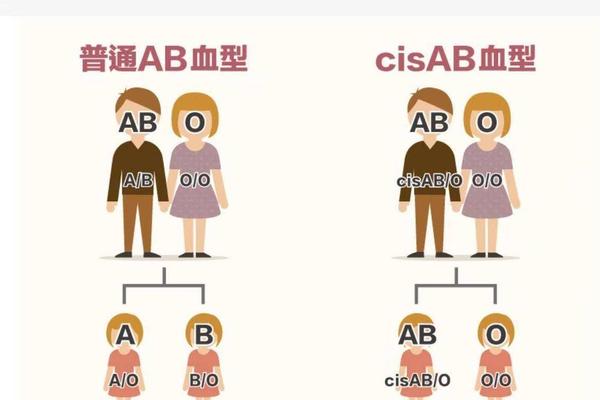
CisAB型的发现彻底改变了传统遗传认知。这种由基因连锁突变导致的特殊血型,使A和B抗原编码基因共同位于同一条染色体上。当CisAB型父亲(基因型CisAB/O)与A型母亲(AA)结合时,子女可能通过遗传CisAB染色体获得AB型。上海血液中心曾报道一例AB型父亲与O型母亲生育AB型子女的案例,基因测序证实父亲携带CisAB基因,其发生概率仅为58万分之一。这类案例不仅需要科普教育,更需医疗机构建立快速鉴别机制。
未来研究的探索方向
当前血型遗传研究正从表型观察转向分子机制深度解析。全基因组关联研究(GWAS)已发现7个非ABO基因座与血型抗原表达相关,其中FUT2基因的多态性可解释12%的AB亚型变异。基因编辑技术的突破为血型改造带来可能,2024年北京大学团队利用CRISPR-Cas9在造血干细胞中成功敲除B抗原基因,为AB型向A型的定向转化提供了实验依据。
在临床应用层面,建立中国人群血型基因数据库成为迫切需求。现有血型遗传数据多基于欧洲人群,而我国汉族AB型人群中CisAB型占比达0.17%,显著高于白种人群。开发快速血型基因分型试剂盒,将有助于解决基层医院对特殊血型的识别困境。2024年国家卫健委已将"罕见血型分子诊断标准化"列入临床检验技术发展规划,预计三年内实现三级医院全覆盖。
生命的密码从来不是简单的排列组合。当AB型血液在AB与A型父母构建的遗传通道中流淌时,它既印证着孟德尔定律的精妙,也彰显着生命系统的复杂性。从基因的量子跃迁到社会的认知革命,这个特殊的血型组合犹如棱镜,折射出科学探索中确定性与不确定性的永恒博弈。未来,随着单细胞测序和表观遗传学的发展,我们或许能解开更多血型谜题,但在当下,保持对生命奥秘的敬畏,或许比急于寻求答案更为重要。


