当父母血型存在差异时,新生儿的健康风险往往成为家庭关注的焦点。以母亲O型血、父亲A型血的组合为例,宝宝的血型可能为A型或O型,其中A型血新生儿因母婴ABO血型不合,存在发生溶血性黄疸的风险。数据显示,这类新生儿中约12%-13.6%会出现溶血性黄疸,其中22%可能发展为需要换血的严重病例。这一现象不仅涉及遗传学规律,更与新生儿胆红素代谢机制密切相关,需要从科学角度深入探讨。
血型遗传机制与溶血风险
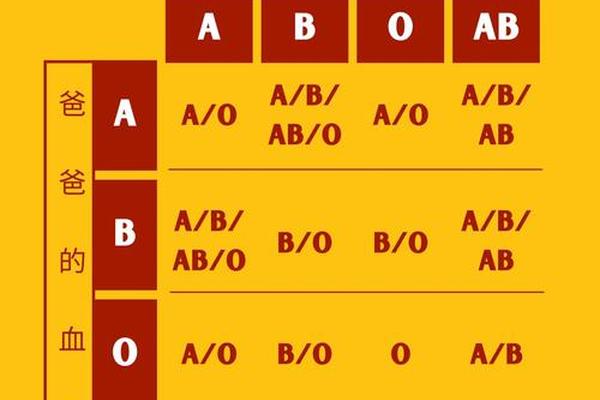
父母血型对子女血型的决定遵循孟德尔遗传定律。母亲O型血(基因型OO)与父亲A型血(基因型AA或AO)结合时,子代可能继承的基因组合为AO或OO,对应A型或O型血。若胎儿为A型血,其红细胞表面的A抗原会与母体血液中的抗A抗体发生免疫反应。这种反应始于孕期——少量胎儿红细胞通过胎盘进入母体循环系统,刺激母体产生IgG型抗体,这些抗体再次通过胎盘进入胎儿体内,引发红细胞破坏。
值得注意的是,并非所有ABO血型不合都会导致严重溶血。研究表明,O型血母亲体内天然存在的抗A、抗B抗体以IgM为主,而IgM无法通过胎盘屏障,只有当抗体转化为IgG时才会引发胎儿溶血。这种转化概率约为20%,且溶血程度与抗体效价、胎盘通透性等因素密切相关。
病理机制与临床表现
溶血性黄疸的核心病理过程是红细胞破裂释放过量胆红素。正常新生儿每日产生胆红素约8.5mg/kg,而溶血患儿可达12-15mg/kg。当未结合胆红素超过肝脏代谢能力时,就会在皮肤、黏膜沉积形成黄疸。重症病例中,游离胆红素可穿透血脑屏障,引发核黄疸(胆红素脑病),导致运动障碍、听力丧失等不可逆损伤。
临床表现呈现显著差异性:
临床数据显示,及时干预可使95%的ABO溶血患儿避免换血治疗。但若延误治疗,约3%的患儿可能遗留神经系统后遗症。
医疗干预的关键节点
现代医学建立了分级诊疗体系应对溶血性黄疸:
1. 光疗阈值动态管理:根据出生时龄制定差异化标准
2. 换血指征把控:当胆红素超过25mg/dL或出现神经系统症状时,需进行双倍血容量换血
3. 辅助治疗创新:静脉注射免疫球蛋白可阻断Fc受体介导的溶血过程,使38%的患儿免于换血
值得注意的是,民间流传的日光疗法、中药浴等替代疗法对溶血性黄疸无效。研究证实,日光中有效蓝光波段不足医院专业设备的10%,且存在紫外线灼伤风险;茵栀黄制剂虽能促进胆红素排泄,但可能引发严重腹泻导致电解质紊乱。
预防策略与家庭监护
产前预防体系包含三大核心:
产后监护要点需要家庭与医疗团队协同:
1. 出生后24小时内开始胆红素监测,建立个体化生长曲线
2. 母乳喂养频次需达到8-12次/日,促进胆红素通过肠道排出
3. 使用经皮胆红素测定仪进行居家监测,数值超过第95百分位时立即就医
研究展望与社会意义
现有研究表明,基因编辑技术可能在未来阻断ABO抗原表达,动物实验已实现50%的血型抗原沉默。基于机器学习的黄疸预测模型,通过分析胎便排出时间、喂养量等12项参数,可将重症预测准确率提升至89%。这些技术进步将为溶血性黄疸防治带来革命性突破。
从公共卫生角度看,建立全国性新生儿溶血病登记系统、完善Rh阴性血型冷冻库网络、开展育龄夫妇血型普查等措施,可使严重病例发生率降低70%。这不仅关乎个体家庭幸福,更是提高人口质量的重要举措。
母婴ABO血型差异引发的溶血性黄疸,既是遗传学特殊案例,也是围产医学的经典课题。通过理解血型遗传规律、掌握病理机制、严格执行分级诊疗方案,多数患儿可获得良好预后。未来研究应聚焦精准预防技术开发,而家庭医疗教育的深化,则是避免治疗延误的最后防线。这需要医学科普工作者、临床医生和科研人员的共同努力,为新生儿健康筑起多重保障。


