在ABO血型系统中,A型血指红细胞表面携带A抗原的血型,而Rh血型系统则以是否存在D抗原来区分阳性或阴性。当一个人同时满足「A型」和「Rh阴性」时,其血型被称为「A型Rh阴性血」,即俗称的「熊猫血」中的一种。这类血型在汉族人群中占比不足0.3%,属于典型的稀有血型。
从抗原分布来看,A型Rh阴性血的特殊性体现在双重稀有性叠加。ABO血型由第9号染色体上的基因控制,而Rh血型由第1号染色体上的RHD和RHCE基因决定。A型Rh阴性血的形成需要个体同时携带A抗原表达的显性基因(如AA或AO基因型)以及RhD抗原缺失的隐性纯合基因(dd基因型)。这种遗传组合的概率极低,导致其临床用血资源极度匮乏。
二、遗传机制与基因突变的影响
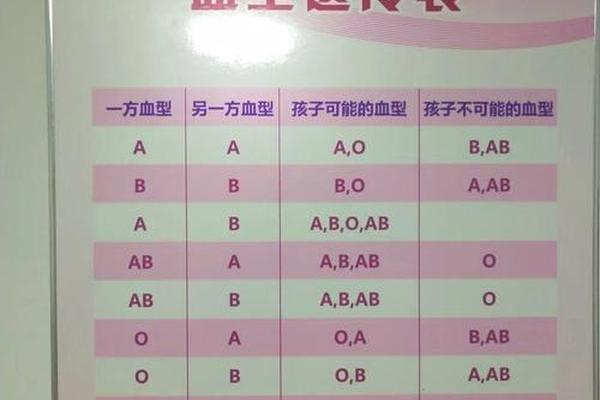
A型Rh阴性血的遗传遵循孟德尔定律。若父母双方均为Rh阴性(dd基因型),则子女必然为Rh阴性;若父母一方为携带者(Dd基因型),子女有50%概率继承隐性基因。例如,若父亲为A型Rh阳性(Dd),母亲为O型Rh阴性(dd),子女可能继承A型基因和d基因,从而成为A型Rh阴性血。
值得注意的是,某些稀有血型的产生与基因突变相关。例如,cisAB血型是由于ABO基因座的突变导致A、B基因出现在同一条染色体上,此类突变可能进一步与Rh阴性基因耦合,形成更复杂的稀有血型。日本学者还发现,核辐射等环境因素可能诱导血型基因突变,如Langereis和Junior血型的出现,这提示A型Rh阴性血的形成也可能受多因素影响。
三、临床输血挑战与抗体风险
Rh阴性血型患者若输入Rh阳性血液,体内可能产生抗D抗体。对于A型Rh阴性血患者而言,这种风险更具特殊性:首次输血后产生的抗体会导致后续只能用Rh阴性血液,而A型Rh阴性血的稀缺性可能延误治疗。例如,Rhnull血型(即完全缺失Rh系统抗原)患者一生仅能接受一次输血,因抗Rh29抗体的产生将彻底阻断后续输血可能。
交叉配血的复杂性也加剧了挑战。除ABO和Rh系统外,还需检测Kidd、Kell等次要血型系统抗体。2016年一项研究显示,约15%的稀有血型患者因抗体筛查失败导致输血延迟。对于A型Rh阴性血患者,需建立个人抗体档案,以便快速匹配合格血源。
四、社会支持系统与解决方案
目前中国各省市血液中心已开展稀有血型库建设,但数据孤岛问题突出。例如,陕西宝鸡市曾发现cisAB血型案例,但此类信息未实现全国联网共享。解金辉等专家呼吁建立区域性调配机制,通过区块链技术实现血源动态追踪,这可将应急响应时间缩短50%以上。
对于A型Rh阴性血人群,自体储血和互助献血是重要补充。健康成年人每半年可捐献400毫升全血,冷冻保存技术可使红细胞存活10年以上。基因编辑技术为人工合成通用型血液提供了可能。2023年英国剑桥大学团队利用CRISPR技术敲除红细胞表面的抗原基因,成功培育出「O型Rh阴性」人造血液,未来或可扩展至其他稀有血型。
五、总结与展望
A型Rh阴性血作为双重稀有血型,其临床价值与社会意义远超生物学范畴。从基因筛查到血库建设,从抗体管理到技术创新,需要构建多维度保障体系。建议推进三方面工作:一是立法强制新生儿稀有血型筛查并建立终身档案;二是完善全国联网的「熊猫血」数据库;三是加强基因工程研究,突破人造血液的技术瓶颈。唯有如此,才能真正破解「用血难」的困局,为生命筑起更坚固的防线。



