当一位O型血的母亲迎来A型血的宝宝,这份新生命带来的喜悦中可能潜藏着一项需要警惕的健康风险——新生儿ABO溶血性黄疸。这种由母婴血型不合引发的病理性黄疸,虽不意味着必然发生严重并发症,但其潜在危害仍值得每个家庭深入了解与科学应对。数据显示,约12%-13.6%的足月新生儿可能发生此类黄疸,其中近1/5可能发展为需要医疗干预的重症。
血型冲突的生物学机制
母婴ABO血型不合导致黄疸的核心机制在于母体免疫系统对胎儿红细胞的攻击。当O型血母亲怀有A型胎儿时,母体血液中的抗A抗体会通过胎盘进入胎儿体内,与胎儿红细胞表面的A抗原结合,引发红细胞破裂(溶血),释放大量胆红素。
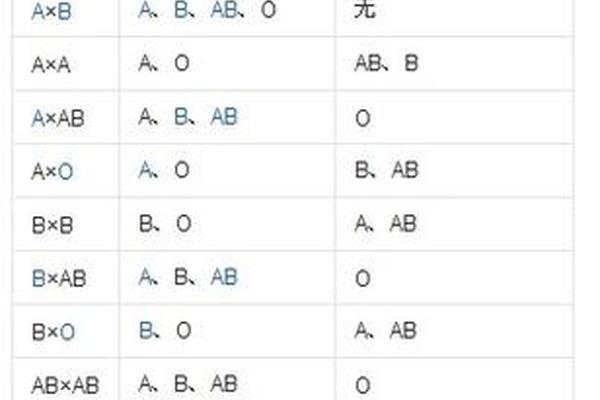
这一过程并非必然发生。自然界中广泛存在的A型血物质(如某些植物、细菌)可能使部分O型血女性在孕前已产生抗A抗体。研究显示,仅有2%-5%的ABO血型不合妊娠会引发明显溶血反应。胎儿的自我保护机制也起到缓冲作用,如胎盘屏障的选择性通透性、胎儿红细胞抗原发育不完全等,都降低了严重溶血的发生概率。
临床特征与早期识别
ABO溶血性黄疸的临床表现具有显著特征性。患儿通常在出生后24小时内即出现黄疸,较生理性黄疸早1-2天,且进展迅速,可能在48小时内达到需干预的临界值。皮肤黄染常从面部向躯干、四肢蔓延,严重者甚至可见巩膜及手足心黄染。
诊断需结合实验室检查:直接抗人球蛋白试验阳性率约60%-80%,血清游离抗体检测与抗体释放试验具有更高特异性。值得注意的是,约30%患儿同时存在贫血,血红蛋白可能降至100-120g/L,网织红细胞计数升高提示代偿性增生。临床案例显示,贵州某医院曾收治黄疸值达17mg/dl的A型血新生儿,经检测发现合并G6PD缺乏症,提示多因素叠加可能加剧病情。
阶梯式医疗干预体系
针对不同严重程度的ABO溶血性黄疸,现代医学已建立成熟的阶梯式治疗方案。光疗作为首选措施,通过波长425-475nm的蓝光将脂溶性胆红素转化为水溶性异构体,其干预阈值根据出生时龄动态调整:出生24小时内>6mg/dl,24-48小时>9mg/dl,48-72小时>12mg/dl。
对于重症病例(胆红素>25mg/dl或每小时上升>0.5mg/dl),换血疗法可快速清除致敏红细胞和抗体。北京某三甲医院数据显示,规范光疗可使90%以上病例避免换血。药物治疗方面,静脉注射免疫球蛋白(0.5-1g/kg)能阻断Fc受体介导的溶血过程,白蛋白输注可增加胆红素结合容量。
产前预防与监测策略
预防ABO溶血性黄疸的关键在于产前系统管理。建议O型血孕妇从孕12周起定期监测抗A(B)IgG抗体效价:
山东大学附属医院研究显示,中药干预(如茵陈蒿汤)可使抗体效价降低1-2个滴度,配合维生素E等抗氧化剂使用效果更佳。对于有流产史或前胎溶血史的孕妇,孕20周后需加强胎儿超声监测,观察有无皮肤水肿、肝脾肿大等征象。
家庭护理的科学认知
出院后的家庭护理需要把握科学尺度。日光浴可作为辅助手段,但需注意:
1. 选择上午10点前、下午4点后,避免紫外线伤害

2. 每日累计照射不超过1小时,分2-3次进行
3. 遮盖眼睛及生殖器,裸晒面积不超过体表30%
喂养方面,母乳喂养可促进胎便排出,但重度溶血时需暂停母乳24-48小时。上海市儿童医院研究显示,添加益生菌(如宝乐安)可使胆红素日均下降幅度提高15%。
医学认知的更新与展望
近年研究揭示了更多影响ABO溶血严重程度的因素。内蒙古医科大学附属医院发现,UGT1A1基因多态性影响胆红素代谢效率,携带TA7等位基因的患儿更易发生高胆红素血症。未来可能通过基因筛查实现个体化干预。纳米吸附技术、单克隆抗体疗法等新型治疗手段正在临床试验阶段,有望进一步降低换血治疗比例。
面对母婴血型不合带来的挑战,现代医学已建立起从预防、诊断到治疗的全链条解决方案。通过规范的产前监测、及时的新生儿筛查和科学的家庭护理,绝大多数ABO溶血性黄疸患儿都能获得良好预后。重要的是建立理性认知——既不过度恐慌,也不轻视潜在风险,在医患协作中为每个新生命筑牢健康防线。


